thêm 15g NaOH nguyên chất vào 65g dung dịch NaOH 5% có sẵn. Nồng độ % của dung dịch mới là

Những câu hỏi liên quan
1.Cho 15g NaOH và 65g NaCl.Tính nồng độ phần trăm của NaOH và NaCl trong dung dịch mới.
2.Xác định nồng độ phần trăm của dung dịch thu được khi hòa tan 36g Na2CO3 ngậm 10 phân tử nước và 185 ml H2O.
mk làm câu 2,câu 1 hình như thiếu (sai)
câu 2
\(n_{Na_2CO_3.10H_2O}=\dfrac{36}{286}=\dfrac{18}{143}mol\)
=> mNa2CO3=18/143 . 106=13,34 gam
mdd=36+185=221 gam ( vì D H2O=1g/ml)
=> C% =6%
Đúng 1
Bình luận (0)
1.Biết độ tan của muối ăn ở 40 °C là 71g.Tính nồng độ phần trăm của dung dịch muối ăn bão hòa.
2.Cho 15g NaOH và 65g NaCl.Tính nồng độ phần trăm của NaOH và NaCl trong dung dịch mới.
3.Xác định nồng độ phần trăm của dung dịch thu được khi hòa tan 36g Na2CO3 ngậm 10 phân tử nước và 185 ml H2O.
1. mdd=mct+mdm=71+100=171(g)
ADCT: C%=mct/mdd×100%
→=71/171×100%=41,52%
Đúng 0
Bình luận (0)
Câu 1:
Nồng độ phần trăm của dung dịch muối ăn bão hòa ở nhiệt độ 40oC:
\(C\%_{ddNaCl}=\dfrac{m_{NaCl}}{m_{ddNaCl}}.100\%\\ =\dfrac{m_{NaCl}}{m_{NaCl}+m_{dm}}.100\%\\ =\dfrac{71}{71+100}.100=41,52\%\)
Đúng 0
Bình luận (0)
khối lượng dung dịch là
mđ=mct+md71+100=171(g)
nồng độ phần trăm của dung dịch bão hòa là
C%=\(\dfrac{mct}{mdd}\).100%
C%=\(\dfrac{71}{171}\).100= 41,52%
Đúng 0
Bình luận (0)
Nhiệt phân hoàn toàn 15g muối cacbonat của 1 kim loại hóa trị II. Dẫn hết khí sinh ra vào 200g dung dịch NaOH 4% vừa đủ thì thu được dung dịch mới có nồng độ các chất tan là 6,63%. Xác định công thức muối đem nhiệt phân? A.
C
a
C
O
3
B.
M
g
C
O
3
C.
B
a
C
O
3
D.
S
r...
Đọc tiếp
Nhiệt phân hoàn toàn 15g muối cacbonat của 1 kim loại hóa trị II. Dẫn hết khí sinh ra vào 200g dung dịch NaOH 4% vừa đủ thì thu được dung dịch mới có nồng độ các chất tan là 6,63%. Xác định công thức muối đem nhiệt phân?
A. C a C O 3
B. M g C O 3
C. B a C O 3
D. S r C O 3

Khối lượng dung dịch sau phản ứng:
m d d = 200 + 44 x ( g a m )
Ta có phương trình về tổng nồng độ các chất:
84. ( 2 x − 0,2 ) + 106. ( 0,2 − x ) 200 + 44 x .100 = 0,0663 ⇔ x = 0,15
Phân tử khối của muỗi đem nhiệt phân là: M = 15 0,15 = 100 ( g / m o l ) .
Vậy muối là C a C O 3
⇒ Chọn A.
Đúng 0
Bình luận (0)
Tính nồng độ % chất tan NaOH khi trộn 150g dung dịch NaOH 20% với 220g dung dịch NaOH 15%. Phải thêm bao nhiêu gram chất tan vào dung dịch đó để có được dung dịch NaOH 30%
\(m_{NaOH}=150\cdot20\%+220\cdot15\%=63\left(g\right)\)
\(C\%_{NaOH}=\dfrac{63}{150+220}\cdot100\%=17.02\%\)
Để : thu được dung dịch NaOH 30%
\(m_{NaOH\left(tv\right)}=a\left(g\right)\)
\(C\%_{NaOH\left(30\%\right)}=\dfrac{63+a}{370+a}\cdot100\%=30\%\)
\(\Rightarrow a=68.57\left(g\right)\)
Đúng 3
Bình luận (0)
- Áp dụng phương pháp đường chéo :
\(\Rightarrow\dfrac{150}{220}=\dfrac{x-15}{20-x}\)
=> x = 17%
- Áp dụng phương pháp đường chéo :
=> x = 68,7g
Vậy ...
Đúng 2
Bình luận (0)
Bài 1. Có sẵn 60 gam dung dịch NaOH 20%. Tính nồng độ % của dung dịch thu được khi:a. Pha thêm 40 gam nước.b.cô cạn bớt 10 gam nước. Bài 2. Có sẵn 60 gam dung dịch HNO3 20%. Tính nồng độ % của dung dịch thu được khi:a. Pha thêm 200 gam nước.b. Cô cạn bớt 400 gam nước.Bài 3. Có sẵn 400 gam dung dịch H2SO4 19,6%. Tính nồng độ % của dung dịch thu được khi:a. Pha thêm 200 gam nước.b. Cô cạn bớt 100 gam nước.
Đọc tiếp
Bài 1. Có sẵn 60 gam dung dịch NaOH 20%. Tính nồng độ % của dung dịch thu được khi:
a. Pha thêm 40 gam nước.
b.cô cạn bớt 10 gam nước.
Bài 2. Có sẵn 60 gam dung dịch HNO3 20%. Tính nồng độ % của dung dịch thu được khi:
a. Pha thêm 200 gam nước.
b. Cô cạn bớt 400 gam nước.
Bài 3. Có sẵn 400 gam dung dịch H2SO4 19,6%. Tính nồng độ % của dung dịch thu được khi:
a. Pha thêm 200 gam nước.
b. Cô cạn bớt 100 gam nước.
Bài 1 :
a)
$m_{NaOH} = 60.20\% = 12(gam)$
$m_{dd} = 60 + 40 = 100(gam)$
$C\%_{NaOH} = \dfrac{12}{100}.100\% = 12\%$
b)
$m_{dd} = 60 - 10 = 50(gam)$
$C\%_{NaOH} = \dfrac{12}{50}.100\% = 24\%$
Bài 2 :
a)
$m_{HNO_3} = 60.20\% = 12(gam)$
$m_{dd} = 60 + 200 = 260(gam)$
$C\%_{HNO_3} = \dfrac{12}{260}.100\% = 4,62\%$
b) Khi cô cạn 400 gam nước thì không còn nước trong dd trên nên không tồn tại dd
Đúng 2
Bình luận (0)
Bài 3 :
a) $m_{H_2SO_4} = 400.19,6\% = 78,4(gam)$
$m_{dd} = 400 + 200 = 600(gam)$
$C\%_{H_2SO_4} = \dfrac{78,4}{600}.100\% = 13,1\%$
b) $m_{dd} = 400 - 100 = 300(gam)$
$C\%_{H_2SO_4} = \dfrac{78,4}{300}.100\% = 26,13\%$
Đúng 2
Bình luận (0)
Bài 2:
a) mHNO3= 20%.60=12(g)
Khi thêm 200 gam nước:
\(C\%ddHNO3\left(mới\right)=\dfrac{12}{200+60}.100\approx46,154\%\)
b) Cô cạn 400 gam nước?? Dung dịch có 60 gam thôi ạ!
Đúng 1
Bình luận (0)
có sẵn 45gam dung dịch NaOH 15%. Tính nồng độ dung dịch thu được khi thêm 20ml nước
`D_{H_2O}=1(g//ml)`
`->m_{H_2O}=1.20=20(g)`
`m_{NaOH}=45.15\%=6,75(g)`
`->C\%_{NaOH\ sau}={6,75}/{45+20}.100\%\approx 10,38\%`
Đúng 2
Bình luận (0)
Thêm 240ml dung dịch NaOH 1M vào một cốc thuỷ tinh đựng 100ml dung dịch AlCl3 nồng độ x mol/l, khuấy đều đến phản ứng hoàn toàn thấy trong cốc có 0,08 mol chất kết tủa. Thêm tiếp 100ml dung dịch NaOH 1M vào cốc, khuấy đều đến phản ứng hoàn toàn thấy trong cốc có 0,06 mol chất kết tủa. Nồng độ x là A. 0,75M B. 1M C. 0,5M D. 0,8M
Đọc tiếp
Thêm 240ml dung dịch NaOH 1M vào một cốc thuỷ tinh đựng 100ml dung dịch AlCl3 nồng độ x mol/l, khuấy đều đến phản ứng hoàn toàn thấy trong cốc có 0,08 mol chất kết tủa. Thêm tiếp 100ml dung dịch NaOH 1M vào cốc, khuấy đều đến phản ứng hoàn toàn thấy trong cốc có 0,06 mol chất kết tủa. Nồng độ x là
A. 0,75M
B. 1M
C. 0,5M
D. 0,8M
Phản ứng đầu không có kết tủa bị hòa tan, phản ứng sau có kết tủa bị hòa tan (nếu cả 2 phản ứng đều có kết tủa bị hòa tan thì số mol NaOH chênh lệch giữa 2 lần phải bằng số mol kết tủa chênh lệch của 2 lần)
Lần 2:
n A l ( O H ) 3 = 0 , 06 ⇒ n A l ( O H ) = 0 , 34 - 0 , 06 . 3 4 = 0 , 04 ⇒ n A l C l 3 = 0 , 06 + 0 , 04 = 0 , 1 ⇒ x = 1
Đáp án B
Đúng 0
Bình luận (0)
Xác định nồng độ phần trăm của các dung dịch trong các trường hợp sau:
a. Pha thêm 20g nước vào 80g dung dịch muối ăn có nồng độ 15%.
b. Trộn 200g dung dịch muối ăn có nồng độ 20% với 300g dung dich muối ăn có nồng độ 5%.
c. Trộn 100g dung dịch NaOH a% với 50g dung dịch NaOH 10% được dung dịch NaOH 7,5%.
a)m dd sau=100gam
mNaCl không đổi=80.15%=12 gam
C% dd NaCl sau=12/100.100%=12%
b)mdd sau=200+300=500 gam
Tổng mNaCl sau khi trộn=200.20%+300.5%=55 gam
C% dd NaCl sau=55/500.100%=11%
c) mdd sau=150 gam
mNaOH trg dd 10%=5 gam
mNaOH trong dd sau khi trộn=150.7,5%=11,25 gam
=>mNaOH trong dd a%=11,25-5=6,25 gam
=>C%=a%=6,25/100.100%=6,25% => a=6,25
Đúng 1
Bình luận (0)
a)m dd sau=100gam
mNaCl không đổi=80.15%=12 gam
C% dd NaCl sau=12/100.100%=12%
b)mdd sau=200+300=500 gam
Tổng mNaCl sau khi trộn=200.20%+300.5%=55 gam
C% dd NaCl sau=55/500.100%=11%
c) mdd sau=150 gam
mNaOH trg dd 10%=5 gam
mNaOH trong dd sau khi trộn=150.7,5%=11,25 gam
=>mNaOH trong dd a%=11,25-5=6,25 gam
=>C%=a%=6,25/100.100%=6,25% => a=6,25
Đúng 0
Bình luận (0)
Cho m gam Al tan hoàn toàn vào dung dịch chứa y mol HCl thu được dung dịch A chứa 2 chất tan có nồng độ mol bằng nhau. Thêm từ từ dung dịch NaOH vào dung dịch A, đồ thị biểu diễn số mol kết tủa Al(OH)3 phụ thuộc vào số mol NaOH thêm vào như sau: Giá trị của m là A. 4,05. B. 8,10. C. 5,40. D. 6,75.
Đọc tiếp
Cho m gam Al tan hoàn toàn vào dung dịch chứa y mol HCl thu được dung dịch A chứa 2 chất tan có nồng độ mol bằng nhau. Thêm từ từ dung dịch NaOH vào dung dịch A, đồ thị biểu diễn số mol kết tủa Al(OH)3 phụ thuộc vào số mol NaOH thêm vào như sau:
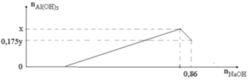 Giá trị của m là
Giá trị của m là
A. 4,05.
B. 8,10.
C. 5,40.
D. 6,75.
Đáp án C
PTHH: 2Al + 6HCl → 2AlCl3 + 3H2 (1)
NaOH + HCl → NaCl + H2O (2)
3NaOH + AlCl3 → 3NaCl + Al(OH)3 (3)
NaOH + Al(OH)3 → NaAlO2 + 2H2O (4)
Trong A: n A l C l 3 = m/27 = x (mol) (*); n H C l d ư = y – 3m/27 = x (mol)
→ Theo giả thiết: m/27 = y – 3m/27 → y = 4m/27 (**)
Khi n A l ( O H ) 3 = x → n N a O H = 4x
Khi n A l ( O H ) 3 = 0,175y → n N a O H = x + 4x – 0,175y = 0,86 (mol)
Thay (*) và (**) vào → m = 5,4 gam
Đúng 0
Bình luận (0)
Cho m gam Al tan hoàn toàn vào dung dịch chứa y mol HCl thu được dung dịch A chứa 2 chất tan có nồng độ mol bằng nhau. Thêm từ từ dung dịch NaOH vào dung dịch A, đồ thị biểu diễn số mol kết tủa Al(OH)3 phụ thuộc vào số mol NaOH thêm vào như sau: Giá trị của m là A. 4,05 B. 8,10 C. 5,40 D. 6,75
Đọc tiếp
Cho m gam Al tan hoàn toàn vào dung dịch chứa y mol HCl thu được dung dịch A chứa 2 chất tan có nồng độ mol bằng nhau. Thêm từ từ dung dịch NaOH vào dung dịch A, đồ thị biểu diễn số mol kết tủa Al(OH)3 phụ thuộc vào số mol NaOH thêm vào như sau: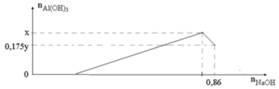
Giá trị của m là
A. 4,05
B. 8,10
C. 5,40
D. 6,75
PTHH: 2Al + 6HCl → 2AlCl3 + 3H2 (1)
NaOH + HCl → NaCl + H2O (2)
3NaOH + AlCl3 → 3NaCl + Al(OH)3 (3)
NaOH + Al(OH)3 → NaAlO2 + 2H2O (4)
Trong A: n(AlCl3) = m/27 = x (mol) (*); n(HCl)dư = y – 3m/27 = x (mol)
→ Theo giả thiết: m/27 = y – 3m/27 → y = 4m/27 (**)
Khi n(Al(OH)3) = x → n(NaOH) = 4x
Khi n(Al(OH)3) = 0,175y → n(NaOH) = x + 4x – 0,175y = 0,86 (mol)
Thay (*) và (**) vào → m = 5,4 gam → Đáp án C
Đúng 0
Bình luận (0)






















